自从2017年8月首个CART细胞疗法上市以来,CART治疗就已经逐渐成为了癌症在治疗的热门疗法。CART疗法在白血病和淋巴瘤的治疗领域展现了非常不错的治疗效果。诺华(Novartis)的Kymriah和吉利德(Gilead)的Yescarta都已在美国和欧盟获批上市,但目前的T细胞疗法被证明难以应用于像乳腺癌和肺癌这样的实体肿瘤。
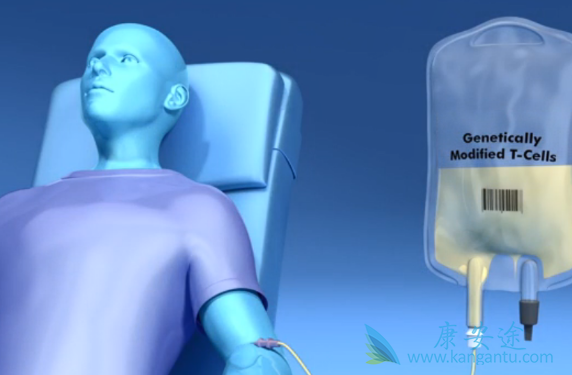
T细胞是在体内循环的特异性免疫细胞,可以识别并杀死包括癌细胞在内的异常细胞,而T细胞疗法的关键在于获得大量的可以识别癌症细胞的T细胞。目前主要使用过继性T细胞疗法(ACT),分为两类,一是从癌症组织分离出可以识别癌症细胞的T细胞,二是从患者血液中分离T细胞,在体外用癌症抗原诱导T细胞识别癌症抗原,或是进行基因编辑靶向一种表达肿瘤细胞表面的蛋白。两者都需经过体外增殖,最后输回患者体内。这就是一个标准的CART细胞治疗的流程
目前的T细胞疗法用于实体肿瘤时,往往无法引发足够强的免疫反应;而如果同时使用细胞因子增强免疫反应,因为所有的T细胞都会得到刺激,所以会产生严重的炎症等副作用。为了克服这些局限性,辅助ACT治疗实体肿瘤,MIT生物工程和材料科学与工程教授,Torque公司联合创始人,Darrell Irvine博士领导的团队为T细胞设计了一种全新纳米胶体,可以负载100倍的药量。该纳米胶体“药物背包”一种蛋白质纳米胶体颗粒,由交联分子和细胞因子IL-15组成。“药物背包”通过交联分子连接在从肿瘤部位提取的T细胞表面。当T细胞识别并与靶细胞(癌细胞)抗原相互作用时,引发T细胞表面的还原电位升高,导致交联分子被降解,从而使细胞因子IL-15得以释放去增强免疫反应。这一结果于近期发表在《Nature Biotechnology》》杂志上。
















请简单描述您的疾病情况,我们会有专业的医学博士免费为您解答问题(24小时内进行电话回访)