
结直肠癌已经成为发病率位居世界第三的恶性肿瘤,数据显示,我国结肠癌的发病率十年间翻了近一番,而30岁以下青年人患者比例占到了15%。年轻人越来越多得 直肠癌 ?结直肠癌是一种比较典型的富贵病,跟我们的生活条件和饮食方式息息相关。年轻人患结直肠 ...
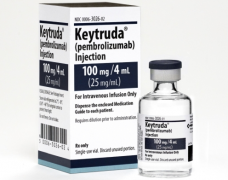
2014年9月和12月,默沙东和百时美施贵宝的PD-1单抗Keytruda (pembrolizumab) 和Opdivo (nivolumab)率先在美国获得批准。之后,这类药物单用以及与其他药物联用进行癌症治疗一直是肿瘤研发的热点。自2015年药审改革以来,中国的原研新药获得了政策和资本 ...
PD-1对于没有基因突变的肺癌患者是一个好的治疗方法。晚期肺癌患者的5年生存期终于有了大幅度提高,从历史的4%提高到了16%,肺癌似乎不再那么可怕,新药物将给更多患者带来福音。近年来,随着一些新药的出现,对部分患者而言,肺癌并不可怕:经过基因检 ...
肺癌是全世界死亡率最高的肿瘤,没有之一。据统计,2015年中国新发肺癌病例73万,死亡60万,名副其实的癌症第一杀手。研究人员分析了16位活过5年的患者情况,很多临床数据都说明抽烟的患者更容易从PD-1抗体治疗中获益。其中10位患者从确诊到使用Opdivo治 ...
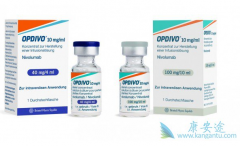
代号为CA209-003的临床试验,是一个多中心的一期临床试验,2009年一月正式开始招募患者,2013年4月结束,一共招募了129名多线治疗失败的晚期非小细胞肺癌患者,使用PD-1抗体Opdivo治疗,剂量包括1/3/10 mg/kg三组,2周一次,最长使用时间96周。5年生存率 ...
PD-1抑制剂治疗需要多久起效?一般建议第一次接受PD-1治疗三个月作为一个周期评估,如果用药PD-1抗体以后三个月评估效果显着瘤体缩小或者控制没有再次进展副作用也可控范围内那么建议持续用药2年。FDA的药品评价和研究中心中血液学和肿瘤产品室主任Richa ...

美国食品药物管理局(FDA)批准两个CAR-T细胞产品用于治疗B细胞来源血液肿瘤。而近期,诺华(Novartis)、吉利德(Kite,)、朱诺(Juno)三家公司公布的CAR-T细胞治疗复发难治B细胞淋巴瘤的Ⅱ期研究数据也令人振奋。客观缓解率达到53%~84%,完全缓解(CR)率为40%~ ...

如何进一步维持并提高疗效? 尽管小样本量研究显示,部分患者接受CAR-T细胞治疗后可长期无病存活,但临床实践中仍须面临一部分患者会复发进展。原因可能与细胞在体内存活时间短,肿瘤细胞表面CD19抗原丢失,肿瘤细胞程序性死亡受体配体-1(PD-L1)表达上调 ...
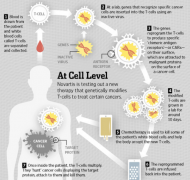
目前,科济公司已经在香港及美国设立了子公司,并且于2016年年底正式在美国启动了临床前的研究,有望于2017年正式获得美国FDA批准开始临床研究。为了更好地保证CAR-T的制备质量,自2016年3月起科济公司严格按照国家药监局注射液的GMP标准建立了3100平方 ...

2015年,在上海市卫计委、上海市肿瘤研究所以及上海市转化医学协同创新中心的支持下,李宗海带领研究团队开展了全球首个针对肝癌的CAR-T临床研究及针对脑胶质瘤的CAR-T临床研究,取得了初步成果。 2015年,李宗海牵头创立的国内首家CAR-T生物医药企 ...
上海实体瘤CAR-T细胞治疗产业化迈出实质步伐。日前,由上海交通大学医学院附属仁济医院上海市肿瘤研究所研究员李宗海获3000万美元融资创立的中国首家CAR-T生物医药企业――科济生物医药(上海)有限公司,正式启用了严格按照国家药监局注射液GMP标准建立 ...
研究证明,那些在使用 Keytruda 前接受过任何放疗的患者,相比于未接受过放疗的患者,疾病进展风险可降低44%,死亡风险降低42%。这些抗肿瘤效果更明显地体现在接受颅外放射的患者身上。 《Lancet Oncology》杂志也曾发表KEYNOTE-001试验的后续 ...
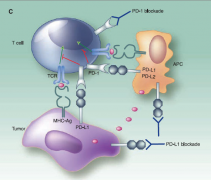
PD-1 /PD-L1联合化疗,肺鳞癌:2018年3月20日,罗氏公司公布,相比单独使用化疗,PD-L1抑制剂TECENTRIQ (atezolizumab) 联合化疗 (卡铂+白蛋白结合型紫杉醇)一线治疗晚期肺鳞癌患者,可以降低疾病恶化/死亡风险。 非鳞状非小细胞肺癌:PD-1抑制 ...

随着癌症领域科学研究的深入以及药物研发的不断投入,癌症治疗从化疗、靶向治疗,发展到免疫治疗,不断延长患者的生存时间以及提高患者的生活质量。今年公布的ASCO癌症2018进展中提到, PD-1 /PD-L1抗体的出现,每年可以挽救25万肺癌患者的生命。但是, ...

PD-1 抑制剂就像一匹从中脱颖而出的黑马。从2014年7月,第一个PD-1抑制剂上市,到现在只有三年余。PD-1抑制剂创造了制药史上的奇迹,陆续获批恶性黑色素瘤、非小细胞肺癌、肾癌、头颈鳞癌、肝癌、胃癌、霍奇金淋巴瘤等适应症,也造福了许多肿瘤患者。 ...
目前, PD-1 抑制剂免疫治疗与化疗、小分子靶向治疗是患者及医生同行经常讨论的一个热门话题。当前我们应用的阻断PD-1的免疫检查点抑制剂方法,实际上以解放免疫T细胞,来抵抗肿瘤,在于激发自身的免疫潜能。然而PD-1抑制剂仅对部分患者有效,但它一旦起 ...

近年来,以 CAR-T 技术为代表的肿瘤免疫治疗成为引领未来医学革命的先进治疗技术,备受瞩目。 特别是2017年8月31日FDA批准世界首个CAR-T治疗药物Kymriah (CTL019)上市, 成为细胞治疗的里程碑事件。在这一事件的推动下, 国内很多从事细胞治疗行业的科学 ...
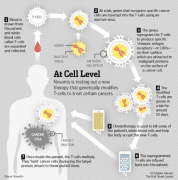
人类肿瘤治疗史上的里程碑无疑一定有一座是肿瘤免疫疗法的。而肿瘤免疫疗法的主要两大领域, 细胞治疗 以及以PD1/PDL1为代表的免疫检查点抑制剂都在飞速发展。目前,已经有5种抗PD1/PDL1抗体药物上市,包括默沙东的Keytruda、百时美施贵宝的Opdivo、罗氏 ...
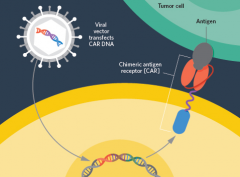
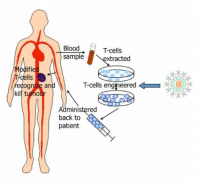
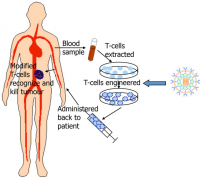
简单来说, CAR-T 疗法是从患者体内分离出T细胞,在体外对T细胞进行改造,为其装上能够特异性识别癌细胞的“导航”――嵌合抗原受体(CAR)后,再将这类“改装后的CAR-T细胞”进行扩增,回输到患者体内,发挥特异的抗癌作用。(Credit: UT Southwestern ...
尽管ACT激活T细胞会导致一定程度的免疫刺激和炎症,但是CD-19特异性,BCMA特异性和CD-22特异性 CAR-T 细胞均观察到严重的细胞因子释放并发症(CRS)。该症状较TIL-和TCR疗法常见的流行性感冒样并发症更加严重。CAR T细胞引发的CRS严重程度与肿瘤负担相关。 ...
免费咨询电话:4000 980 586
微信咨询

扫描二维码
免费咨询医学博士